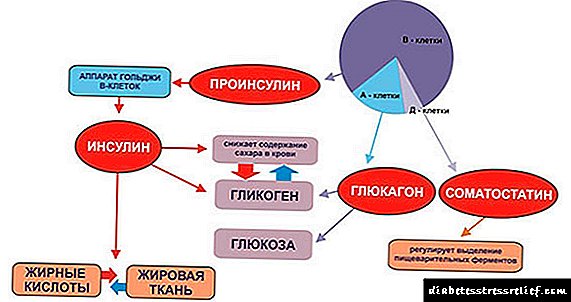
கொலஸ்ட்ரால் தொகுப்பின் கட்டுப்பாடு
கொழுப்பின் தொகுப்பின் கட்டுப்பாடு - அதன் முக்கிய நொதி (HMG-CoA ரிடக்டேஸ்) வெவ்வேறு வழிகளில் மேற்கொள்ளப்படுகிறது.
எச்.எம்.ஜி ரிடக்டேஸின் பாஸ்போரிலேஷன் / டிஃபோஸ்ஃபோரிலேஷன். இன்சுலின் / குளுகோகன் விகிதத்தில் அதிகரிப்புடன், இந்த நொதி பாஸ்போரிலேட்டுகள் மற்றும் செயலில் உள்ள நிலைக்கு செல்கிறது. இன்சுலின் செயல் 2 என்சைம்கள் மூலம் மேற்கொள்ளப்படுகிறது.
HMG-CoA ரிடக்டேஸ் கைனேஸ் பாஸ்பேடேஸ், இது கைனேஸை செயலற்ற டிஃபோஸ்ஃபோரிலேட்டட் நிலையாக மாற்றுகிறது:
பாஸ்போடேஸ் HMG-CoA ரிடக்டேஸை டிஃபோஸ்ஃபோரிலேட்டட் ஆக்டிவ் ஸ்டேட்டாக மாற்றுவதன் மூலம். இந்த எதிர்விளைவுகளின் விளைவாக HMG-CoA ரிடக்டேஸின் டிஃபோஸ்ஃபோரிலேட்டட் செயலில் உள்ள வடிவம் உருவாகிறது.
இதன் விளைவாக, உறிஞ்சும் காலத்தில், கொழுப்பு அதிகரிக்கிறது. இந்த காலகட்டத்தில், கொழுப்பு - அசிடைல் - கோஏ (கார்போஹைட்ரேட்டுகள் மற்றும் கொழுப்புகள் அடங்கிய உணவை உண்ணுவதன் விளைவாக, குளுக்கோஸ் மற்றும் கொழுப்பு அமிலங்களின் முறிவின் போது அசிடைல் கோஏ உருவாகும்போது) ஆரம்ப மூலக்கூறின் கிடைக்கும் தன்மையும் அதிகரிக்கிறது.
Postabsorbent நிலையில், புரோட்டீங்கனேஸ் A மூலம் குளுகோகன் HMG - CoA - ரிடக்டேஸின் பாஸ்போரிலேஷனைத் தூண்டுகிறது, அதை செயலற்ற நிலையாக மாற்றுகிறது. அதே நேரத்தில் குளுகோகன் HMG-CoA ரிடக்டேஸின் பாஸ்போடேஸின் பாஸ்போரிலேஷன் மற்றும் செயலற்ற தன்மையைத் தூண்டுகிறது, இதனால் HMG-CoA ரிடக்டேஸை ஒரு பாஸ்போரிலேட்டட் செயலற்ற நிலையில் வைத்திருக்கிறது. இதன் விளைவாக, பிந்தைய உறிஞ்சுதல் காலத்திலும், உண்ணாவிரதத்திலும் கொலஸ்ட்ராலின் தொகுப்பு எண்டோஜெனஸ் தொகுப்பு மூலம் தடுக்கப்படுகிறது. உணவில் உள்ள கொழுப்பின் அளவு 2% ஆகக் கொண்டுவரப்பட்டால், எண்டோஜெனஸ் கொலஸ்ட்ராலின் தொகுப்பு கூர்மையாகக் குறைந்தது. ஆனால் கொலஸ்ட்ரால் தொகுப்பின் முழுமையான நிறுத்தம் ஏற்படாது.
உணவில் இருந்து வரும் கொலஸ்ட்ராலின் செல்வாக்கின் கீழ் கொலஸ்ட்ரால் உயிரியக்கவியல் தடுப்பதன் அளவு நபருக்கு நபர் மாறுபடும். இது கொலஸ்ட்ரால் உருவாவதற்கான செயல்முறைகளின் தனித்துவத்தைக் குறிக்கிறது. கொலஸ்ட்ரால் தொகுப்பின் தீவிரத்தை குறைப்பதன் மூலம், இரத்தத்தில் அதன் செறிவைக் குறைக்க முடியும்.
உணவுடன் கொழுப்பை உட்கொள்வதற்கும் ஒருபுறம் உடலில் அதன் தொகுப்புக்கும் பித்த அமிலங்கள் மற்றும் கொலஸ்ட்ரால் வெளியேற்றப்படுவதற்கும் இடையிலான சமநிலை உடைந்தால், திசுக்களில் கொழுப்பின் செறிவு மற்றும் இரத்தம் மாறுகிறது. இரத்தக் கொழுப்பின் செறிவு (ஹைபர்கொலெஸ்டிரோலீமியா) அதிகரிப்புடன் மிகவும் கடுமையான விளைவுகள் தொடர்புடையவை, அதே நேரத்தில் பெருந்தமனி தடிப்பு மற்றும் கொலெலித்தியாசிஸ் உருவாகும் வாய்ப்பு அதிகரிக்கிறது.
குடும்ப ஹைபர்கொலெஸ்டிரோலீமியா (எச்.சி.எஸ்) - இந்த வடிவம் மிகவும் பொதுவானது - 200 பேருக்கு 1 நோயாளி. எச்.சி.எஸ்ஸில் மரபுவழி குறைபாடு என்பது எல்.டி.எல் செல்கள் உறிஞ்சப்படுவதை மீறுவதாகும், எனவே எல்.டி.எல் கேடபாலிசத்தின் வீதத்தில் குறைவு ஏற்படுகிறது. இதன் விளைவாக, இரத்தத்தில் எல்.டி.எல் செறிவு உயர்கிறது, அதே போல் எல்.டி.எல் இல் நிறைய இருப்பதால் கொலஸ்ட்ரால். ஆகையால், எச்.சி.எஸ் உடன், திசுக்களில், குறிப்பாக தோலில் (சாந்தோமாஸ்), தமனிகளின் சுவர்களில் கொழுப்பை வைப்பது சிறப்பியல்பு.
HMG-CoA ரிடக்டேஸின் தொகுப்பின் தடுப்பு
கொலஸ்ட்ரால் வளர்சிதை மாற்ற பாதையின் இறுதி தயாரிப்பு. இது HMG-CoA ரிடக்டேஸ் மரபணுவின் படியெடுத்தல் வீதத்தைக் குறைக்கிறது, இதனால் அதன் சொந்த தொகுப்பைத் தடுக்கிறது. கல்லீரல் கொழுப்பிலிருந்து பித்த அமிலங்களை தீவிரமாக ஒருங்கிணைக்கிறது, எனவே பித்த அமிலங்கள் HMG-CoA ரிடக்டேஸ் மரபணுவின் செயல்பாட்டைத் தடுக்கின்றன. சுமார் 3 இன் தொகுப்பிற்குப் பிறகு HMG-CoA ரிடக்டேஸ் இருப்பதால், இந்த கொழுப்பு நொதியின் தொகுப்பைத் தடுப்பது ஒரு பயனுள்ள ஒழுங்குமுறை ஆகும்.
நீங்கள் தேடுவதைக் கண்டுபிடிக்கவில்லையா? தேடலைப் பயன்படுத்தவும்:
கொலஸ்ட்ரால் எஸ்டர் பரிமாற்றம்
கொழுப்பு நிதியில் இலவச கொலஸ்ட்ரால் மற்றும் கொலஸ்ட்ரால் எஸ்டர்கள் உள்ளன, அவை செல்கள் மற்றும் இரத்த லிப்போபுரோட்டின்களில் காணப்படுகின்றன.
பகுதி II வளர்சிதை மாற்றம் மற்றும் ஆற்றல்
உயிரணுக்களில், அசைல்-கோஏ-கொலஸ்ட்ரால்-அசைல்ட்ரான்ஸ்ஃபெரேஸ் (ஏசிஏஏடி) இன் செயல்பாட்டின் மூலம் கொழுப்பின் மதிப்பீடு ஏற்படுகிறது:
அசைல்-கோஏ + கொலஸ்ட்ரால் - * எச்.எஸ்-கோஏ + அசைல்கொலெஸ்டிரால்
மனித உயிரணுக்களில், லினோலில்கொலெஸ்டிரால் முக்கியமாக உருவாகிறது. இலவச கொழுப்பைப் போலன்றி, உயிரணு சவ்வுகளில் உள்ள அதன் எஸ்டர்கள் மிகக் குறைந்த அளவுகளில் உள்ளன மற்றும் முக்கியமாக லிப்பிட் சொட்டுகளின் ஒரு பகுதியாக சைட்டோசோலில் காணப்படுகின்றன. ஈஸ்டர்களின் உருவாக்கம் ஒருபுறம், சவ்வுகளிலிருந்து அதிகப்படியான கொழுப்பை அகற்றுவதற்கான ஒரு பொறிமுறையாகவும், மறுபுறம், கலத்தில் கொழுப்பை சேமிப்பதற்கான ஒரு பொறிமுறையாகவும் கருதலாம். கொலஸ்ட்ரால் எஸ்டர்களை ஹைட்ரோலைஸ் செய்யும் எஸ்டெரேஸ் என்சைம்களின் பங்கேற்புடன் வள அணிதிரட்டல் நிகழ்கிறது:
அசைல்கொலெஸ்டிரால் + எச் 2 ஓ - * கொழுப்பு அமிலம் + கொலஸ்ட்ரால்
எஸ்டர்களின் தொகுப்பு மற்றும் நீராற்பகுப்பு பல உயிரணுக்களில் நிகழ்கிறது, ஆனால் குறிப்பாக அட்ரீனல் கோர்டெக்ஸின் உயிரணுக்களில் செயல்படுகிறது: இந்த உயிரணுக்களில் 80% வரை கொழுப்புகள் எஸ்டர்களால் குறிக்கப்படுகின்றன, மற்ற உயிரணுக்களில் இது பொதுவாக 20% க்கும் குறைவாகவே இருக்கும்.
இரத்த லிபோன்ரோட்டின்களில் எஸ்டர்களின் உருவாக்கம் லெசித்தின்-கொலஸ்ட்ரால் அசைல்ட்ரான்ஸ்ஃபெரேஸ் (எல்.எச்.ஏ.டி) பங்கேற்புடன் நடைபெறுகிறது, இது அசைல் எச்சத்தை லெசித்தின் ஐ-நிலையில் இருந்து கொலஸ்ட்ராலுக்கு மாற்றுவதை ஊக்குவிக்கிறது (படம் 10.31). வெவ்வேறு லிப்போபுரோட்டின்களுக்கான எஸ்டெரிஃபிகேஷன் விகிதம் கணிசமாக வேறுபட்டது மற்றும் இது LHAT ஐ (முக்கியமாக apo-AT, அதே போல் CI) செயல்படுத்தும் அல்லது இந்த நொதியைத் தடுக்கும் (C-II) தடுக்கும் அபோலிபோபுரோட்டின்களின் இருப்பைப் பொறுத்தது. வேண்டும் olee அனைத்து புரதங்கள் 2/3. பெரிய கோலை மரியாதைகள் உருவாக்கப்பட்டது ஒலீயிக் மற்றும் லினோலிக் அமிலங்கள் எஸ்டர்ஸ்களையும் கொண்டதாகும். மற்ற லிப்போபுரதங்கள் எஸ்டர் உருவாக்கம் ஹெச்டிஎல் காட்டிலும் மெதுவான விகிதத்தில் ஏற்படுகிறது.
படம். 10.31. LHAT இன் செயல்பாட்டின் கீழ் கொலஸ்ட்ரால் எஸ்டர்களின் உருவாக்கம்
எல்.எச்.ஏ.டி எச்.டி.எல்லின் மேற்பரப்பு அடுக்கில் மொழிபெயர்க்கப்பட்டுள்ளது மற்றும் பாஸ்போலிபிட் மோனோலேயரில் உள்ள கொழுப்பை ஒரு அடி மூலக்கூறாகப் பயன்படுத்துகிறது. இங்கு உருவாகும் கொழுப்பு எஸ்டர்கள், அவற்றின் முழுமையான ஹைட்ரோபோபசிட்டி காரணமாக, மோசமாக தக்கவைக்கப்படுகின்றன
பாடம் 10. வளர்சிதை மாற்றம் மற்றும் லிப்பிட் செயல்பாடு
பாஸ்போலிபிட் மோனோலேயர் மற்றும் லிப்போபுரோட்டினின் லிப்பிட் மையத்தில் மூழ்கியது. அதே நேரத்தில், பாஸ்போலிப்பிட் மோனோலேயரில் கொலஸ்ட்ராலுக்கான இடம் விடுவிக்கப்படுகிறது, இது உயிரணு சவ்வுகளிலிருந்து அல்லது பிற லிப்போபுரோட்டின்களிலிருந்து கொழுப்பை நிரப்ப முடியும். இதனால், எல்.எச்.ஏ.டி செயல்பாட்டின் விளைவாக எச்.டி.எல் ஒரு கொழுப்பு பொறியாகத் தோன்றுகிறது.
பித்த அமில தொகுப்பு
கல்லீரலில், கொழுப்பின் ஒரு பகுதி பித்த அமிலங்களாக மாற்றப்படுகிறது. காலிக் அமிலங்கள் கோலனிக் அமிலத்தின் வழித்தோன்றல்களாக கருதப்படலாம் (படம் 10.32).
இது போன்ற சோலனிக் அமிலம் உடலில் உருவாகவில்லை. ஹெபடோசைட்டுகளில், கொழுப்பு நேரடியாக செனோடொக்சிகோலிக் மற்றும் கோலிக் அமிலங்களை உருவாக்குகிறது - முதன்மை பித்த அமிலங்கள் (படம் 10.33, படம் 10.12 ஐயும் காண்க).
கொலஸ்ட்ரால் உயிரியக்கவியல்
எண்டோபிளாஸ்மிக் ரெட்டிகுலத்தில் கொலஸ்ட்ரால் உயிரியக்கவியல் ஏற்படுகிறது. மூலக்கூறில் உள்ள அனைத்து கார்பன் அணுக்களின் மூலமும் அசிடைல்-எஸ்சிஓஏ ஆகும், இது மைட்டோகாண்ட்ரியாவிலிருந்து சிட்ரேட்டின் ஒரு பகுதியாக வருகிறது, கொழுப்பு அமிலங்களின் தொகுப்பைப் போல. கொலஸ்ட்ரால் உயிரியக்கவியல் 18 ஏடிபி மூலக்கூறுகளையும் 13 என்ஏடிபிஎச் மூலக்கூறுகளையும் பயன்படுத்துகிறது.
கொழுப்பின் உருவாக்கம் 30 க்கும் மேற்பட்ட எதிர்விளைவுகளில் நிகழ்கிறது, அவை பல நிலைகளில் தொகுக்கப்படலாம்.
1. மெவலோனிக் அமிலத்தின் தொகுப்பு.
முதல் இரண்டு தொகுப்பு எதிர்வினைகள் கெட்டோஜெனீசிஸ் எதிர்விளைவுகளுடன் ஒத்துப்போகின்றன, ஆனால் 3-ஹைட்ராக்ஸி -3-மெத்தில்ல்க்ளூடரில்-ஸ்கோஏவின் தொகுப்புக்குப் பிறகு, நொதி நுழைகிறது ஹைட்ராக்ஸிமெதில்-குளுட்டரில்-ஸ்கோஏ ரிடக்டேஸ் (HMG-SCOA ரிடக்டேஸ்), மெவலோனிக் அமிலத்தை உருவாக்குகிறது.
 |
கொலஸ்ட்ரால் தொகுப்பு எதிர்வினை திட்டம்2. ஐசோபென்டெனில் டைபாஸ்பேட்டின் தொகுப்பு. இந்த கட்டத்தில், மூன்று பாஸ்பேட் எச்சங்கள் மெவலோனிக் அமிலத்துடன் இணைக்கப்படுகின்றன, பின்னர் அது டிகார்பாக்சிலேட்டட் மற்றும் டீஹைட்ரஜனேற்றப்படுகிறது. 3. ஐசோபென்டெனில் டைபாஸ்பேட்டின் மூன்று மூலக்கூறுகளை இணைத்த பிறகு, ஃபார்னெசில் டைபாஸ்பேட் ஒருங்கிணைக்கப்படுகிறது. 4. இரண்டு ஃபார்னெசில் டைபாஸ்பேட் எச்சங்கள் பிணைக்கப்படும்போது ஸ்குவாலினின் தொகுப்பு ஏற்படுகிறது. 5. சிக்கலான எதிர்விளைவுகளுக்குப் பிறகு, நேரியல் ஸ்கொலீன் லானோஸ்டெரோலுக்கு சுழற்சி செய்கிறது. 6. அதிகப்படியான மீதில் குழுக்களை அகற்றுதல், மூலக்கூறின் மறுசீரமைப்பு மற்றும் ஐசோமரைசேஷன் ஆகியவை கொழுப்பின் தோற்றத்திற்கு வழிவகுக்கிறது. ஹைட்ராக்ஸிமெதில்க்ளூடரில்-எஸ்-கோஏ ரிடக்டேஸின் செயல்பாட்டைக் கட்டுப்படுத்துதல்3. கொழுப்பு உயிரியக்கவியல் வீதமும் செறிவைப் பொறுத்தது குறிப்பிட்ட கேரியர் புரதம்ஹைட்ரோபோபிக் இடைநிலை தொகுப்பு வளர்சிதை மாற்றங்களின் பிணைப்பு மற்றும் போக்குவரத்துக்கு வழங்குகிறது. நீங்கள் உங்கள் கருத்தை கேட்கலாம் அல்லது விடலாம். ஒழுங்குமுறையின் முக்கிய புள்ளி மெவலோனிக் அமிலத்தின் உருவாக்கத்தின் எதிர்வினை. 1. அலோஸ்டெரிக் கட்டுப்பாடு. கொழுப்பு, மற்றும் கல்லீரலில் - மற்றும் பித்த அமிலங்கள் HMG-CoA ரிடக்டேஸைத் தடுக்கின்றன. 2. HMG-CoA ரிடக்டேஸ் கொழுப்பின் தொகுப்பின் அடக்குமுறை. 3. HMG-CoA ரிடக்டேஸின் பாஸ்போரிலேஷன்-டிஃபோஸ்ஃபோரிலேஷன் மூலம் கட்டுப்பாடு, செயலில் பாஸ்போரிலேட்டட் வடிவம். குளுகோகன் செயலிழக்கச் செய்கிறது, மற்றும் இன்சுலின் எதிர்வினைகளின் சிக்கலான அடுக்கின் மூலம் செயல்படுத்துகிறது. இதனால், கொழுப்புத் தொகுப்பின் வீதம் உறிஞ்சக்கூடிய மற்றும் பிந்தைய உறிஞ்சுதல் நிலைகளில் மாற்றத்துடன் மாறுகிறது. 4. கல்லீரலில் HMG-CoA ரிடக்டேஸின் தொகுப்பு விகிதம் தெளிவான தினசரி ஏற்ற இறக்கங்களுக்கு உட்பட்டது: நள்ளிரவில் அதிகபட்சம், மற்றும் காலையில் குறைந்தபட்சம். கொலஸ்ட்ரால் எஸ்டர் பரிமாற்றம் கலங்களில் வெளிப்படும் போது கொலஸ்ட்ரால் மதிப்பீடு செய்யப்படுகிறது அசைல் CoA இல் கொழுப்பு acyltransferase (ACAT): அசைல்-கோஏ + கொலஸ்ட்ரால் ® என்எஸ்-கோஏ + அசைல்கொலெஸ்டிரால் உயிரணுக்களில், முக்கியமாக லினோலில்கொலெஸ்டிரால் உருவாகிறது. லிப்பிட் துளிகளின் ஒரு பகுதியாக சைட்டோசோலில் எஸ்டர்கள் முக்கியமாக காணப்படுகின்றன. ஒருபுறம், சவ்வுகளில் இருந்து அதிகப்படியான கொழுப்பை அகற்றுவதற்கான ஒரு பொறிமுறையாகவும், மறுபுறம், கலத்தில் கொழுப்பை சேமிப்பதற்கான ஒரு பொறிமுறையாகவும் எஸ்டர்களின் உருவாக்கம் கருதப்படலாம். என்சைம்களின் பங்கேற்புடன் இருப்புக்களை அணிதிரட்டுகிறது esteraseஹைட்ரோலைசிங் கொழுப்பு எஸ்டர்கள்: அசைல்கொலெஸ்டிரால் + எச்2O ® கொழுப்பு அமிலம் + கொழுப்பு எஸ்டர்களின் தொகுப்பு மற்றும் நீராற்பகுப்பு குறிப்பாக அட்ரீனல் கோர்டெக்ஸின் உயிரணுக்களில் செயல்படுகிறது. இரத்த லிப்போபுரோட்டின்களில் ஈஸ்டர் உருவாக்கம் பங்கேற்புடன் நிகழ்கிறது லெசித்தின்-கொழுப்பு acyltransferase (LHAT), அசைல் எச்சத்தை லெசித்தின் இருந்து கொழுப்புக்கு மாற்றுவதை ஊக்குவிக்கிறது. LHAT கல்லீரலில் உருவாகிறது, இரத்த ஓட்டத்தில் சுரக்கிறது மற்றும் லிப்போபுரோட்டின்களுடன் இணைக்கப்படுகிறது. எச்.டி.எல் இல் மிகவும் சுறுசுறுப்பான எல்.எச்.ஏ.டி, இது மேற்பரப்பு அடுக்கில் மொழிபெயர்க்கப்பட்டுள்ளது. இங்கு உருவாகும் கொலஸ்ட்ரால் எஸ்டர்கள் ஹைட்ரோபோபிக் மற்றும் லிப்பிட் கோரில் மூழ்கியுள்ளன. பாஸ்போலிபிட் மோனோலேயரில், கொழுப்புக்கான இலவச இடம் உள்ளது, இது உயிரணு சவ்வுகளிலிருந்து அல்லது பிற லிப்போபுரோட்டின்களிலிருந்து கொழுப்பை நிரப்பலாம். இதனால், எல்.எச்.ஏ.டி செயல்பாட்டின் விளைவாக எச்.டி.எல் ஒரு கொழுப்பு பொறியாகத் தோன்றுகிறது. பித்த அமில தொகுப்பு கல்லீரலில், கொழுப்பின் ஒரு பகுதி பித்த அமிலங்களாக மாற்றப்படுகிறது. பித்த அமிலங்கள் கோலனிக் அமிலத்தின் வழித்தோன்றல்களாக கருதப்படலாம். இது போன்ற சோலனிக் அமிலம் உடலில் உருவாகவில்லை. கொழுப்பிலிருந்து வரும் ஹெபடோசைட்டுகளில், முதன்மை பித்த அமிலங்கள் உருவாகின்றன - chenodeoxycholic மற்றும் cholic. குடல் தாவரங்களின் நொதிகளின் செயல்பாட்டின் கீழ் குடலுக்குள் பித்தம் சுரந்த பிறகு, அவர்களிடமிருந்து இரண்டாம் பித்த அமிலங்கள் உருவாகின்றன - lithocholic மற்றும் deoxycholic. அவை குடலில் இருந்து உறிஞ்சப்படுகின்றன, போர்டல் நரம்பின் இரத்தம் கல்லீரலுக்குள் நுழைகிறது, பின்னர் பித்தத்திற்குள் செல்கிறது. பித்தத்தில் முக்கியமாக இணைந்த பித்த அமிலங்கள் உள்ளன, அதாவது, கிளைசின் அல்லது டாரினுடன் அவற்றின் சேர்மங்கள். பித்தத்தில் பித்த அமிலங்களின் செறிவு சுமார் 1% ஆகும். பித்த அமிலங்களின் முக்கிய பகுதி இதில் ஈடுபட்டுள்ளது ஹெபடோஎன்டெரிக் சுழற்சி.பித்த அமிலங்களின் ஒரு சிறிய பகுதி - ஒரு நாளைக்கு சுமார் 0.5 கிராம் - மலத்தில் வெளியேற்றப்படுகிறது. கல்லீரலில் புதிய பித்த அமிலங்களின் தொகுப்பால் இது ஈடுசெய்யப்படுகிறது, பித்த அமில நிதி சுமார் 10 நாட்களில் புதுப்பிக்கப்படுகிறது. கொலஸ்ட்ரால் முக்கியமாக குடல்கள் வழியாக வெளியேற்றப்படுகிறது. இது பித்தத்தின் ஒரு பகுதியாக உணவு மற்றும் கல்லீரலில் இருந்து குடலில் நுழைகிறது. இரத்தத்தில் உறிஞ்சப்பட்ட கொழுப்பு பித்தத்திலிருந்து உருவாகும் ஒரு பகுதியைக் கொண்டுள்ளது (எண்டோஜெனஸ் கொழுப்புகல்லீரலில் ஒருங்கிணைக்கப்பட்டது), மற்றும் உணவில் இருந்து பெறப்பட்ட பின்னம் (வெளிப்புற கொழுப்பு). திசுக்களில் இருந்து கொழுப்பை அகற்றுவது கல்லீரலில் உள்ள பித்த அமிலங்களுக்கு ஆக்ஸிஜனேற்றப்படுவதன் மூலமும், பின்னர் அவை மலம் (ஒரு நாளைக்கு சுமார் 0.5 கிராம்) வெளியேற்றப்படுவதாலும், மாறாத கொழுப்பை வெளியேற்றுவதன் மூலமும் (மலம் கூட) ஏற்படுகிறது. நிலையான நிலையில்: (கொழுப்புமுடிவு + கொழுப்புIND) - (கொழுப்புekskr + பித்த அமிலங்கள்ekskr) = 0 இந்த சமநிலை தொந்தரவு செய்தால், திசுக்களிலும் இரத்தத்திலும் கொழுப்பின் செறிவு மாறுகிறது. அதிகரித்த இரத்தக் கொழுப்பு - ஹைபர்கொலஸ்ட்ரலோமியாவைக். இது பெருந்தமனி தடிப்பு மற்றும் பித்தப்பை நோய்க்கான வாய்ப்பை அதிகரிக்கிறது. லிப்பிட் எக்சேஞ்ச் ரெகுலேஷன் லிப்பிட் வளர்சிதை மாற்றம் மத்திய நரம்பு மண்டலத்தால் கட்டுப்படுத்தப்படுகிறது. நீண்ட காலம் நீடிக்கும் எதிர்மறை உணர்ச்சி மன அழுத்தம், இரத்த ஓட்டத்தில் கேடகோலமைன்களின் வெளியீட்டின் அதிகரிப்பு குறிப்பிடத்தக்க எடை இழப்பை ஏற்படுத்தும். விளைவு குளுக்கோஜென் லிபோலிடிக் அமைப்பில் கேடகோலமைன்களின் செயலுக்கு ஒத்ததாகும். அட்ரினலின் மற்றும் நோரெபினிஃப்ரைன் திசு லிபேஸின் செயல்பாட்டை அதிகரிக்கவும், கொழுப்பு திசுக்களில் லிபோலிசிஸின் வீதத்தை அதிகரிக்கவும், இதன் விளைவாக, இரத்த பிளாஸ்மாவில் உள்ள கொழுப்பு அமிலங்களின் உள்ளடக்கம் அதிகரிக்கிறது. இன்சுலின் லிபோலிசிஸ் மற்றும் கொழுப்பு அமிலங்களை அணிதிரட்டுவதில் அட்ரினலின் மற்றும் குளுகோகனின் எதிர் விளைவைக் கொண்டுள்ளது. வளர்ச்சி ஹார்மோன் லிபோலிசிஸைத் தூண்டுகிறது, அசெனிலேட் சைக்லேஸின் தொகுப்பைத் தூண்டுகிறது. பிட்யூட்டரி ஹைபோஃபங்க்ஷன் உடலில் கொழுப்பு படிவதற்கு வழிவகுக்கிறது (பிட்யூட்டரி உடல் பருமன்). தைராக்ஸின், செக்ஸ் ஹார்மோன்கள்லிப்பிட் வளர்சிதை மாற்றத்தையும் பாதிக்கிறது. விலங்குகளில் உள்ள பாலியல் சுரப்பிகளை அகற்றுவது அதிகப்படியான கொழுப்பு படிவதற்கு காரணமாகிறது. லிப்பிட் மெட்டாபாலிக் டிஸார்டர்ஸ் கொழுப்பு என்பது விலங்கு உயிரினங்களுக்கு குறிப்பிட்ட ஒரு ஸ்டீராய்டு ஆகும். மனித உடலில் அதன் உருவாக்கத்தின் முக்கிய இடம் கல்லீரல் ஆகும், அங்கு 50% கொழுப்பு ஒருங்கிணைக்கப்படுகிறது, 15-20% சிறுகுடலில் உருவாகிறது, மீதமுள்ளவை தோல், அட்ரீனல் கோர்டெக்ஸ் மற்றும் கோனாட்களில் ஒருங்கிணைக்கப்படுகின்றன. கொழுப்பு நிதியின் உருவாக்கம் மற்றும் அதன் செலவினங்களின் வழிகள் படம் 22.1 இல் வழங்கப்பட்டுள்ளன. படம். 22.1. உடலில் கொழுப்பின் உருவாக்கம் மற்றும் விநியோகம். மனித உடலின் கொழுப்பு (மொத்தம் சுமார் 140 கிராம்) நிபந்தனையுடன் மூன்று குளங்களாக பிரிக்கலாம்: 30 கிராம்), விரைவாக பரிமாறிக்கொள்ளும், குடல் சுவர், இரத்த பிளாஸ்மா, கல்லீரல் மற்றும் பிற பரன்கிமால் உறுப்புகளின் கொழுப்பைக் கொண்டுள்ளது, புதுப்பித்தல் 30 நாட்களில் நிகழ்கிறது (1 கிராம் / நாள்), 50 கிராம்), மற்ற உறுப்புகள் மற்றும் திசுக்களின் கொழுப்பை மெதுவாக பரிமாறிக்கொள்வது, 60 கிராம்), முதுகெலும்பு மற்றும் மூளை, இணைப்பு திசு ஆகியவற்றின் மிக மெதுவாக பரிமாறிக்கொள்ளப்பட்ட கொழுப்பு, புதுப்பிப்பு வீதம் பல ஆண்டுகளாக கணக்கிடப்படுகிறது. உயிரணுக்களின் சைட்டோசோலில் கொழுப்பின் தொகுப்பு ஏற்படுகிறது. இது மனித உடலில் மிக நீளமான வளர்சிதை மாற்ற பாதைகளில் ஒன்றாகும். இது 3 நிலைகளில் தொடர்கிறது: முதலாவது மெவலோனிக் அமிலத்தின் உருவாக்கத்துடன் முடிவடைகிறது, இரண்டாவதாக ஸ்குவலீன் (30 கார்பன் அணுக்களைக் கொண்ட நேரியல் ஹைட்ரோகார்பன் அமைப்பு) உருவாகிறது. மூன்றாவது கட்டத்தின் போது, ஸ்குவாலீன் ஒரு லானோஸ்டெரால் மூலக்கூறாக மாற்றப்படுகிறது, பின்னர் லானோஸ்டெரோலை கொலஸ்ட்ராலாக மாற்றும் 20 தொடர்ச்சியான எதிர்வினைகள் உள்ளன. சில திசுக்களில், கொலஸ்ட்ராலின் ஹைட்ராக்சைல் குழு எஸ்டர்களை உருவாக்குகிறது. எதிர்வினை உள்விளைவு நொதி AHAT (அசைல்கோஏ: கொலஸ்ட்ரால் அசைல்ட்ரான்ஸ்ஃபெரேஸ்) மூலமாக வினையூக்கப்படுகிறது. எல்.டி.எச்.டி (லெசித்தின்: கொலஸ்ட்ரால் அசைல்ட்ரான்ஸ்ஃபெரேஸ்) என்ற நொதி அமைந்துள்ள எச்.டி.எல்லில் உள்ள இரத்தத்திலும் எஸ்டெரிஃபிகேஷன் எதிர்வினை ஏற்படுகிறது. கொலஸ்ட்ரால் எஸ்டர்கள் என்பது இரத்தத்தால் கடத்தப்படும் அல்லது உயிரணுக்களில் வைக்கப்படும் வடிவமாகும். இரத்தத்தில், சுமார் 75% கொழுப்பு எஸ்டர்களின் வடிவத்தில் உள்ளது. 3-ஹைட்ராக்ஸி -3-மெத்தில்ல்க்ளூடரில்-கோஏ ரிடக்டேஸ் (HMG-CoA ரிடக்டேஸ்) - செயல்பாட்டின் முக்கிய நொதியின் செயல்பாடு மற்றும் அளவை பாதிப்பதன் மூலம் கொலஸ்ட்ரால் தொகுப்பு கட்டுப்படுத்தப்படுகிறது. இது இரண்டு வழிகளில் அடையப்படுகிறது: 1. HMG-CoA ரிடக்டேஸின் பாஸ்போரிலேஷன் / டிஃபோஸ்ஃபோரிலேஷன். இன்சுலின் HMG-CoA ரிடக்டேஸின் டிஃபோஸ்ஃபோரிலேஷனைத் தூண்டுகிறது, இதன் மூலம் அதை செயலில் உள்ள நிலைக்கு மொழிபெயர்க்கிறது. எனவே, உறிஞ்சும் காலத்தில், கொழுப்பின் தொகுப்பு அதிகரிக்கிறது. இந்த காலகட்டத்தில், அசிடைல்-கோஏ என்ற தொகுப்புக்கான தொடக்க மூலக்கூறின் கிடைக்கும் தன்மையும் அதிகரிக்கிறது. குளுகோகன் எதிர் விளைவைக் கொண்டுள்ளது: புரத கைனேஸ் A மூலம், இது HMG-CoA ரிடக்டேஸின் பாஸ்போரிலேஷனைத் தூண்டுகிறது, அதை செயலற்ற நிலையில் மாற்றுகிறது. இதன் விளைவாக, போஸ்ட்சார்ப்ஷன் காலத்திலும், உண்ணாவிரதத்திலும் கொழுப்பின் தொகுப்பு தடுக்கப்படுகிறது. 2. HMG-CoA ரிடக்டேஸின் தொகுப்பின் தடுப்பு.கொலஸ்ட்ரால் (வளர்சிதை மாற்ற பாதையின் இறுதி தயாரிப்பு) HMG-CoA ரிடக்டேஸ் மரபணுவின் டிரான்ஸ்கிரிப்ஷன் வீதத்தை குறைக்கிறது, இதனால் அதன் சொந்த தொகுப்பைத் தடுக்கிறது, மேலும் பித்த அமிலங்களும் இதேபோன்ற விளைவை ஏற்படுத்துகின்றன. இரத்தத்தின் கொழுப்பு போக்குவரத்து மருந்தின் ஒரு பகுதியாக மேற்கொள்ளப்படுகிறது. எல்பிக்கள் திசுக்களில் வெளிப்புற கொழுப்பை வழங்குகின்றன, உறுப்புகளுக்கு இடையில் அதன் ஓட்டத்தையும் உடலில் இருந்து வெளியேற்றத்தையும் தீர்மானிக்கின்றன. எஞ்சிய சி.எம் இன் ஒரு பகுதியாக கல்லீரலுக்கு வெளிப்புற கொழுப்பு வழங்கப்படுகிறது. அங்கு, ஒருங்கிணைந்த எண்டோஜெனஸ் கொலஸ்ட்ரால் சேர்ந்து, இது ஒரு பொதுவான நிதியை உருவாக்குகிறது. ஹெபடோசைட்டுகளில், TAG கள் மற்றும் கொலஸ்ட்ரால் VLDL இல் தொகுக்கப்படுகின்றன, மேலும் இந்த வடிவத்தில் இரத்தத்தில் சுரக்கப்படுகின்றன. இரத்தத்தில், எல்.ஜி. எல்.டி.எல் என்பது கொழுப்பின் முக்கிய போக்குவரத்து வடிவமாகும், அதில் இது திசுக்களுக்கு வழங்கப்படுகிறது (70% கொழுப்பு மற்றும் இரத்தத்தில் உள்ள அதன் எஸ்டர்கள் எல்.டி.எல் இன் பகுதியாகும்). இரத்தத்திலிருந்து எல்.டி.எல் கல்லீரல் (75% வரை) மற்றும் பிற திசுக்களில் அவற்றின் மேற்பரப்பில் எல்.டி.எல் ஏற்பிகளைக் கொண்டுள்ளது. கலத்திற்குள் நுழையும் கொழுப்பின் அளவு அதன் தேவையை விட அதிகமாக இருந்தால், எல்.டி.எல் ஏற்பிகளின் தொகுப்பு ஒடுக்கப்படுகிறது, இது இரத்தத்திலிருந்து கொழுப்பின் ஓட்டத்தை குறைக்கிறது. கலத்தில் இலவச கொழுப்பின் செறிவு குறைந்து, மாறாக, ஏற்பி தொகுப்பு செயல்படுத்தப்படுகிறது. எல்.டி.எல் ஏற்பி தொகுப்பை ஒழுங்குபடுத்துவதில் ஹார்மோன்கள் ஈடுபட்டுள்ளன: இன்சுலின், ட்ரையோடோதைரோனைன் மற்றும் பாலியல் ஹார்மோன்கள் ஏற்பிகளின் உருவாக்கத்தை அதிகரிக்கின்றன, மேலும் குளுக்கோகார்ட்டிகாய்டுகள் குறைகின்றன. “கொழுப்பு திரும்பும் போக்குவரத்து” என்று அழைக்கப்படுபவற்றில், அதாவது. கல்லீரலுக்கு கொலஸ்ட்ரால் திரும்புவதை உறுதி செய்யும் பாதை, எச்.டி.எல் முக்கிய பங்கு வகிக்கிறது. அவை கல்லீரலில் முதிர்ச்சியற்ற முன்னோடிகளின் வடிவத்தில் ஒருங்கிணைக்கப்படுகின்றன, அவை நடைமுறையில் கொழுப்பு மற்றும் TAG ஆகியவற்றைக் கொண்டிருக்கவில்லை. இரத்தத்தில் உள்ள எச்.டி.எல் முன்னோடிகள் கொலஸ்ட்ரால் நிறைவுற்றன, மற்ற எல்பி மற்றும் உயிரணு சவ்வுகளிலிருந்து பெறுகின்றன. எச்.டி.எல்-க்கு கொழுப்பை மாற்றுவது அவற்றின் மேற்பரப்பில் அமைந்துள்ள எல்.எச்.ஏ.டி என்சைமை உள்ளடக்கியது. இந்த நொதி பாஸ்பாடிடைல்கோலின் (லெசித்தின்) முதல் கொழுப்பு வரை ஒரு கொழுப்பு அமில எச்சத்தை இணைக்கிறது. இதன் விளைவாக, கொலஸ்ட்ரால் எஸ்டரின் ஒரு ஹைட்ரோபோபிக் மூலக்கூறு உருவாகிறது, இது எச்.டி.எல் உள்ளே நகர்கிறது. இதனால், கொழுப்பால் செறிவூட்டப்பட்ட எச்.டி.எல் குடிக்காமல், எச்.டி.எல் 3 ஆக மாறும் - முதிர்ந்த மற்றும் பெரிய துகள்கள். எச்.டி.எல் 3 வி.எல்.டி.எல் மற்றும் எஸ்.டி.டி ஆகியவற்றில் உள்ள TAG க்கான கொழுப்பு எஸ்டர்களை பரிமாற்றம் செய்யுங்கள், இது ஒரு குறிப்பிட்ட புரதத்தின் பங்கேற்புடன் கொழுப்பு புரோட்டீன்களுக்கு இடையில் கொழுப்பு எஸ்டர்களை மாற்றுகிறது. இந்த வழக்கில், எச்.டி.எல் 3 எச்.டி.எல் 2 ஆக மாறுங்கள், இதன் அளவு TAG குவிப்பதால் அதிகரிக்கிறது. எல்பி-லிபேஸின் செல்வாக்கின் கீழ் வி.எல்.டி.எல் மற்றும் எஸ்.டி.டி.எல் ஆகியவை எல்.டி.எல் ஆக மாற்றப்படுகின்றன, அவை முக்கியமாக கல்லீரலுக்கு கொழுப்பை வழங்குகின்றன. கொலஸ்ட்ராலின் ஒரு சிறிய பகுதி எச்.டி.எல் 2 மற்றும் எச்.டி.எல் கல்லீரலுக்கு வழங்கப்படுகிறது. பித்த அமிலங்களின் தொகுப்பு. கல்லீரலில், ஒரு நாளைக்கு 500–700 மி.கி பித்த அமிலங்கள் கொழுப்பிலிருந்து தொகுக்கப்படுகின்றன. அவற்றின் உருவாக்கம் ஹைட்ராக்சிலேஸின் பங்கேற்புடன் ஹைட்ராக்சைல் குழுக்களை அறிமுகப்படுத்துவதற்கான எதிர்வினைகள் மற்றும் கொழுப்பின் பக்கச் சங்கிலியின் பகுதி ஆக்ஸிஜனேற்றத்தின் எதிர்வினை ஆகியவை அடங்கும் (படம் 22.2): படம். 22.2. பித்த அமிலங்கள் உருவாகும் திட்டம். முதல் தொகுப்பு எதிர்வினை - 7-அ-ஹைட்ராக்சிகோலெஸ்டிரால் உருவாக்கம் - ஒழுங்குமுறை ஆகும். இந்த எதிர்வினைக்கு வினையூக்கும் நொதியின் செயல்பாடு பாதையின் இறுதி தயாரிப்பு, பித்த அமிலங்களால் தடுக்கப்படுகிறது. மற்றொரு ஒழுங்குமுறை பொறிமுறையானது நொதியின் பாஸ்போரிலேஷன் / டிஃபோஸ்ஃபோரிலேஷன் ஆகும் (7-ஏ-ஹைட்ராக்சிலேஸின் பாஸ்போரிலேட்டட் வடிவம் செயலில் உள்ளது). நொதியின் அளவை மாற்றுவதன் மூலமும் ஒழுங்குமுறை சாத்தியமாகும்: கொலஸ்ட்ரால் 7-ஏ-ஹைட்ராக்சிலேஸ் மரபணுவின் படியெடுத்தலைத் தூண்டுகிறது, மேலும் பித்த அமிலங்கள் அடக்குகின்றன. தைராய்டு ஹார்மோன்கள் 7-அ-ஹைட்ராக்சிலேஸின் தொகுப்பைத் தூண்டுகின்றன, மேலும் ஈஸ்ட்ரோஜன் அடக்குமுறை. பித்த அமிலங்களின் தொகுப்பில் ஈஸ்ட்ரோஜனின் இத்தகைய விளைவு ஆண்களை விட 3-4 மடங்கு அதிகமாக பெண்களில் பித்தப்பை நோய் ஏன் ஏற்படுகிறது என்பதை விளக்குகிறது. கொழுப்பிலிருந்து உருவாகும் கோலிக் மற்றும் செனோடொக்சிகோலிக் அமிலங்கள் “முதன்மை பித்த அமிலங்கள்” என்று அழைக்கப்படுகின்றன. இந்த அமிலங்களின் பெரும்பகுதி இணைவுக்கு உட்படுகிறது - பித்த அமிலத்தின் கார்பாக்சைல் குழுவில் கிளைசின் அல்லது டவுரின் மூலக்கூறுகளை சேர்ப்பது. பித்த அமிலங்களின் செயலில் உள்ள வடிவத்துடன் உருவாக்கம் தொடங்குகிறது - CoA இன் வழித்தோன்றல்கள், பின்னர் டாரைன் அல்லது கிளைசின் இணைக்கப்படுகின்றன, இதன் விளைவாக 4 வகைகளின் இணைப்புகள் உருவாகின்றன: டாரோகோலிக் மற்றும் டாரோஹெனோடெக்ஸிகோலிக், கிளைகோகோலிக் மற்றும் கிளைகோஹெனோடாக்சோலிக் அமிலங்கள். அவை அசல் பித்த அமிலங்களைக் காட்டிலும் குறிப்பிடத்தக்க வலுவான குழம்பாக்கிகள். உடலில் டாரினின் அளவு குறைவாக இருப்பதால், கிளைசினுடன் இணைந்தவை டாரைனை விட 3 மடங்கு அதிகமாக உருவாகின்றன. குடலில், பாக்டீரியா நொதிகளின் செயல்பாட்டின் கீழ் முதன்மை பித்த அமிலங்களின் ஒரு சிறிய அளவு இணைப்புகள் இரண்டாம் நிலை பித்த அமிலங்களாக மாற்றப்படுகின்றன. கோலிக்கிலிருந்து உருவாகும் டியோக்ஸிகோலிக் அமிலம் மற்றும் டியோக்ஸிகோலிக் இருந்து உருவாகும் லித்தோகோலிக் ஆகியவை குறைந்த கரையக்கூடியவை மற்றும் குடலில் மெதுவாக உறிஞ்சப்படுகின்றன. குடலுக்குள் நுழையும் பித்த அமிலங்களில் சுமார் 95% போர்டல் நரம்பு வழியாக கல்லீரலுக்குத் திரும்புகின்றன, பின்னர் மீண்டும் பித்தத்தில் சுரக்கப்பட்டு கொழுப்புகளின் குழம்பாக்கலில் மீண்டும் பயன்படுத்தப்படுகின்றன. பித்த அமிலங்களின் இந்த பாதை என்டோஹெபடிக் சுழற்சி என்று அழைக்கப்படுகிறது. மலம் கொண்டு, இரண்டாம் நிலை பித்த அமிலங்கள் பெரும்பாலும் அகற்றப்படுகின்றன. பித்தப்பை நோய் (கோலெலிதியாசிஸ்) என்பது ஒரு நோயியல் செயல்முறையாகும், இதில் பித்தப்பையில் கற்கள் உருவாகின்றன, இதன் அடிப்படை கொழுப்பு. பித்தத்தில் கொழுப்பை வெளியிடுவதோடு பித்த அமிலங்கள் மற்றும் பாஸ்போலிப்பிட்களின் விகிதாசார வெளியீட்டையும் ஹைட்ரோபோபிக் கொழுப்பு மூலக்கூறுகளை மைக்கேலர் நிலையில் வைத்திருக்க வேண்டும். பித்த அமிலங்கள் மற்றும் பித்தத்தில் உள்ள கொழுப்பின் விகிதத்தில் மாற்றத்திற்கு வழிவகுக்கும் காரணங்கள்: கொழுப்பு நிறைந்த உணவு, அதிக கலோரி ஊட்டச்சத்து, பித்தப்பையில் பித்தத்தின் தேக்கம், பலவீனமான என்டோஹெபடிக் சுழற்சி, பித்த அமிலங்களின் பலவீனமான தொகுப்பு, பித்தப்பை தொற்று. கொலலிதியாசிஸ் உள்ள பெரும்பாலான நோயாளிகளில், கொழுப்பின் தொகுப்பு அதிகரிக்கிறது, மேலும் அதிலிருந்து பித்த அமிலங்களின் தொகுப்பு மெதுவாகிறது, இது பித்தத்தில் சுரக்கும் கொழுப்பு மற்றும் பித்த அமிலங்களின் எண்ணிக்கையில் ஏற்றத்தாழ்வுக்கு வழிவகுக்கிறது. இதன் விளைவாக, பித்தப்பையில் கொலஸ்ட்ரால் வீழ்ச்சியடையத் தொடங்குகிறது, இது ஒரு பிசுபிசுப்பு வளிமண்டலத்தை உருவாக்கி படிப்படியாக கடினப்படுத்துகிறது. சில நேரங்களில் இது பிலிரூபின், புரதங்கள் மற்றும் கால்சியம் உப்புகள் ஆகியவற்றால் செறிவூட்டப்படுகிறது. கற்கள் கொலஸ்ட்ரால் (கொலஸ்ட்ரால் கற்கள்) அல்லது கொழுப்பு, பிலிரூபின், புரதங்கள் மற்றும் கால்சியம் ஆகியவற்றின் கலவையை மட்டுமே கொண்டிருக்க முடியும். கொலஸ்ட்ரால் கற்கள் பொதுவாக வெண்மையானவை, கலப்பு கற்கள் வெவ்வேறு நிழல்களில் பழுப்பு நிறத்தில் இருக்கும். கல் உருவாவதற்கான ஆரம்ப கட்டத்தில், செனோடொக்சிகோலிக் அமிலத்தை ஒரு மருந்தாகப் பயன்படுத்தலாம். ஒரு முறை பித்தப்பையில், அது படிப்படியாக கொழுப்பு கற்களைக் கரைக்கும், ஆனால் இது மெதுவான செயல்முறையாகும், இது பல மாதங்கள் நீடிக்கும். பெருந்தமனி தடிப்பு என்பது வாஸ்குலர் சுவரின் உள் மேற்பரப்பில் பெருந்தமனி தட்டுக்களின் தோற்றத்தால் வகைப்படுத்தப்படும் ஒரு நோயியல் ஆகும். இத்தகைய நோயியலின் வளர்ச்சிக்கு ஒரு முக்கிய காரணம், உணவில் இருந்து கொழுப்பை உட்கொள்வது, அதன் தொகுப்பு மற்றும் உடலில் இருந்து வெளியேற்றப்படுவது ஆகியவற்றுக்கு இடையிலான சமநிலையை மீறுவதாகும். பெருந்தமனி தடிப்பு நோயாளிகள் எல்.டி.எல் மற்றும் வி.எல்.டி.எல் செறிவுகளை உயர்த்தியுள்ளனர். எச்.டி.எல் செறிவுக்கும் பெருந்தமனி தடிப்புத் தோல் அழற்சியின் வளர்ச்சிக்கும் இடையே ஒரு தலைகீழ் உறவு உள்ளது. இது திசுக்களில் கொழுப்பின் கேரியர்களாகவும், திசுக்களில் இருந்து எச்.டி.எல் ஆகவும் எல்.டி.எல் செயல்படும் கருத்தாக்கத்துடன் ஒத்துப்போகிறது. பெருந்தமனி தடிப்புத் தோல் அழற்சியின் வளர்ச்சிக்கான அடிப்படை வளர்சிதை மாற்ற "முன்நிபந்தனை" ஹைபர்கொலெஸ்டிரோலீமியா ஆகும். (இரத்தத்தில் அதிக கொழுப்பு). ஹைபர்கொலெஸ்டிரோலீமியா உருவாகிறது: 1. கொழுப்பு, கார்போஹைட்ரேட் மற்றும் கொழுப்புகளை அதிகமாக உட்கொள்வதால், 2. எல்.டி.எல் அல்லது அப்போபி -100 ஏற்பிகளின் கட்டமைப்பில் பரம்பரை குறைபாடுகளைக் கொண்ட ஒரு மரபணு முன்கணிப்பு, அத்துடன் அப்போபி -100 இன் அதிகரித்த தொகுப்பு அல்லது சுரப்பு (குடும்ப ஒருங்கிணைந்த ஹைப்பர்லிபிடெமியா விஷயத்தில், இரத்த செறிவுகள் மற்றும் கொழுப்பு மற்றும் டி.ஏ.ஜி ஆகியவை உயர்த்தப்படுகின்றன). பெருந்தமனி தடிப்பு வளர்ச்சியின் வழிமுறைகளில் ஒரு முக்கிய பங்கு மருந்தின் மாற்றத்தால் செய்யப்படுகிறது. எல்.டி.எல் இல் உள்ள லிப்பிடுகள் மற்றும் புரதங்களின் இயல்பான கட்டமைப்பில் ஏற்படும் மாற்றங்கள் அவை உடலுக்கு அந்நியமாகின்றன, எனவே பாகோசைட்டுகளால் பிடிக்க மிகவும் அணுகக்கூடியவை. மருந்து மாற்றங்கள் பல வழிமுறைகளால் ஏற்படலாம்: 1. இரத்தத்தில் குளுக்கோஸின் செறிவு அதிகரிக்கும் போது ஏற்படும் புரதங்களின் கிளைகோசைலேஷன், 2. பெராக்சைடு மாற்றம், லிப்போபுரோட்டின்களில் லிப்பிட்களில் மாற்றங்கள் மற்றும் அப்போபி -100 இன் கட்டமைப்புக்கு வழிவகுக்கிறது, 3. எல்பி-ஆன்டிபாடியின் ஆட்டோ இம்யூன் வளாகங்களின் உருவாக்கம் (மாற்றப்பட்ட மருந்துகள் ஆட்டோஆன்டிபாடிகளின் உருவாக்கத்தை ஏற்படுத்தும்). மாற்றியமைக்கப்பட்ட எல்.டி.எல் மேக்ரோபேஜ்களால் உறிஞ்சப்படுகிறது. இந்த செயல்முறை குறிப்பிட்ட ஏற்பிகளின் மூலம் உயிரணுக்களுக்குள் நுழைவதைப் போல, உறிஞ்சப்பட்ட கொழுப்பின் அளவைக் கொண்டு கட்டுப்படுத்தப்படுவதில்லை, எனவே மேக்ரோபேஜ்கள் கொலஸ்ட்ரால் அதிக சுமை கொண்டவை மற்றும் துணை நுரையீரல் இடைவெளியில் ஊடுருவிச் செல்லும் “நுரை செல்கள்” ஆக மாறுகின்றன. இது இரத்த நாளங்களின் சுவரில் லிப்பிட் புள்ளிகள் அல்லது கீற்றுகள் உருவாக வழிவகுக்கிறது. இந்த கட்டத்தில், வாஸ்குலர் எண்டோடெலியம் அதன் கட்டமைப்பை பராமரிக்க முடியும். நுரை உயிரணுக்களின் எண்ணிக்கையில் அதிகரிப்புடன், எண்டோடெலியல் சேதம் ஏற்படுகிறது. சேதம் பிளேட்லெட் செயல்படுத்துவதற்கு பங்களிக்கிறது. இதன் விளைவாக, அவை த்ரோம்பாக்ஸானை சுரக்கின்றன, இது பிளேட்லெட் திரட்டலைத் தூண்டுகிறது, மேலும் பிளேட்லெட்-பெறப்பட்ட வளர்ச்சி காரணியை உருவாக்கத் தொடங்குகிறது, இது மென்மையான தசை செல்கள் பெருக்கத்தைத் தூண்டுகிறது. பிந்தையது தமனி சுவரின் உட்புற அடுக்குக்கு இடைக்காலத்திலிருந்து இடம்பெயர்கிறது, இதனால் பிளேக்கின் வளர்ச்சிக்கு பங்களிக்கிறது. மேலும், ஃபைப்ரஸ் திசுக்களுடன் பிளேக் முளைக்கிறது, ஃபைப்ரஸ் மென்படலத்தின் கீழ் உள்ள செல்கள் நெக்ரோடிக், மற்றும் கொலஸ்ட்ரால் இன்டர்செல்லுலர் இடத்தில் வைக்கப்படுகிறது. வளர்ச்சியின் கடைசி கட்டங்களில், பிளேக் கால்சியம் உப்புகளால் செறிவூட்டப்பட்டு மிகவும் அடர்த்தியாகிறது. பிளேக்கின் பகுதியில், இரத்தக் கட்டிகள் பெரும்பாலும் உருவாகின்றன, பாத்திரத்தின் லுமனைத் தடுக்கின்றன, இது தொடர்புடைய திசு தளத்தில் கடுமையான சுற்றோட்ட செயலிழப்பு மற்றும் மாரடைப்பின் வளர்ச்சிக்கு வழிவகுக்கிறது. கொழுப்பின் தொகுப்பின் கட்டுப்பாடு - அதன் முக்கிய நொதி (HMG-CoA ரிடக்டேஸ்) வெவ்வேறு வழிகளில் மேற்கொள்ளப்படுகிறது. எச்.எம்.ஜி ரிடக்டேஸின் பாஸ்போரிலேஷன் / டிஃபோஸ்ஃபோரிலேஷன். இன்சுலின் / குளுகோகன் விகிதத்தில் அதிகரிப்புடன், இந்த நொதி பாஸ்போரிலேட்டுகள் மற்றும் செயலில் உள்ள நிலைக்கு செல்கிறது. இன்சுலின் செயல் 2 என்சைம்கள் மூலம் மேற்கொள்ளப்படுகிறது. HMG-CoA ரிடக்டேஸ் கைனேஸ் பாஸ்பேடேஸ், இது கைனேஸை செயலற்ற டிஃபோஸ்ஃபோரிலேட்டட் நிலையாக மாற்றுகிறது: பாஸ்போடேஸ் HMG-CoA ரிடக்டேஸை டிஃபோஸ்ஃபோரிலேட்டட் ஆக்டிவ் ஸ்டேட்டாக மாற்றுவதன் மூலம். இந்த எதிர்விளைவுகளின் விளைவாக HMG-CoA ரிடக்டேஸின் டிஃபோஸ்ஃபோரிலேட்டட் செயலில் உள்ள வடிவம் உருவாகிறது. இதன் விளைவாக, உறிஞ்சும் காலத்தில், கொழுப்பு அதிகரிக்கிறது. இந்த காலகட்டத்தில், கொழுப்பு - அசிடைல் - கோஏ (கார்போஹைட்ரேட்டுகள் மற்றும் கொழுப்புகள் அடங்கிய உணவை உண்ணுவதன் விளைவாக, குளுக்கோஸ் மற்றும் கொழுப்பு அமிலங்களின் முறிவின் போது அசிடைல் கோஏ உருவாகும்போது) ஆரம்ப மூலக்கூறின் கிடைக்கும் தன்மையும் அதிகரிக்கிறது. Postabsorbent நிலையில், புரோட்டீங்கனேஸ் A மூலம் குளுகோகன் HMG - CoA - ரிடக்டேஸின் பாஸ்போரிலேஷனைத் தூண்டுகிறது, அதை செயலற்ற நிலையாக மாற்றுகிறது. அதே நேரத்தில் குளுகோகன் HMG-CoA ரிடக்டேஸின் பாஸ்போடேஸின் பாஸ்போரிலேஷன் மற்றும் செயலற்ற தன்மையைத் தூண்டுகிறது, இதனால் HMG-CoA ரிடக்டேஸை ஒரு பாஸ்போரிலேட்டட் செயலற்ற நிலையில் வைத்திருக்கிறது. இதன் விளைவாக, பிந்தைய உறிஞ்சுதல் காலத்திலும், உண்ணாவிரதத்திலும் கொலஸ்ட்ராலின் தொகுப்பு எண்டோஜெனஸ் தொகுப்பு மூலம் தடுக்கப்படுகிறது. உணவில் உள்ள கொழுப்பின் அளவு 2% ஆகக் கொண்டுவரப்பட்டால், எண்டோஜெனஸ் கொலஸ்ட்ராலின் தொகுப்பு கூர்மையாகக் குறைந்தது. ஆனால் கொலஸ்ட்ரால் தொகுப்பின் முழுமையான நிறுத்தம் ஏற்படாது. உணவில் இருந்து வரும் கொலஸ்ட்ராலின் செல்வாக்கின் கீழ் கொலஸ்ட்ரால் உயிரியக்கவியல் தடுப்பதன் அளவு நபருக்கு நபர் மாறுபடும். இது கொலஸ்ட்ரால் உருவாவதற்கான செயல்முறைகளின் தனித்துவத்தைக் குறிக்கிறது. கொலஸ்ட்ரால் தொகுப்பின் தீவிரத்தை குறைப்பதன் மூலம், இரத்தத்தில் அதன் செறிவைக் குறைக்க முடியும். உணவுடன் கொழுப்பை உட்கொள்வதற்கும் ஒருபுறம் உடலில் அதன் தொகுப்புக்கும் பித்த அமிலங்கள் மற்றும் கொலஸ்ட்ரால் வெளியேற்றப்படுவதற்கும் இடையிலான சமநிலை உடைந்தால், திசுக்களில் கொழுப்பின் செறிவு மற்றும் இரத்தம் மாறுகிறது. இரத்தக் கொழுப்பின் செறிவு (ஹைபர்கொலெஸ்டிரோலீமியா) அதிகரிப்புடன் மிகவும் கடுமையான விளைவுகள் தொடர்புடையவை, அதே நேரத்தில் பெருந்தமனி தடிப்பு மற்றும் கொலெலித்தியாசிஸ் உருவாகும் வாய்ப்பு அதிகரிக்கிறது. குடும்ப ஹைபர்கொலெஸ்டிரோலீமியா (எச்.சி.எஸ்) - இந்த வடிவம் மிகவும் பொதுவானது - 200 பேருக்கு 1 நோயாளி. எச்.சி.எஸ்ஸில் மரபுவழி குறைபாடு என்பது எல்.டி.எல் செல்கள் உறிஞ்சப்படுவதை மீறுவதாகும், எனவே எல்.டி.எல் கேடபாலிசத்தின் வீதத்தில் குறைவு ஏற்படுகிறது. இதன் விளைவாக, இரத்தத்தில் எல்.டி.எல் செறிவு உயர்கிறது, அதே போல் எல்.டி.எல் இல் நிறைய இருப்பதால் கொலஸ்ட்ரால். ஆகையால், எச்.சி.எஸ் உடன், திசுக்களில், குறிப்பாக தோலில் (சாந்தோமாஸ்), தமனிகளின் சுவர்களில் கொழுப்பை வைப்பது சிறப்பியல்பு. HMG-CoA ரிடக்டேஸின் தொகுப்பின் தடுப்பு கொலஸ்ட்ரால் வளர்சிதை மாற்ற பாதையின் இறுதி தயாரிப்பு. இது HMG-CoA ரிடக்டேஸ் மரபணுவின் படியெடுத்தல் வீதத்தைக் குறைக்கிறது, இதனால் அதன் சொந்த தொகுப்பைத் தடுக்கிறது. கல்லீரல் கொழுப்பிலிருந்து பித்த அமிலங்களை தீவிரமாக ஒருங்கிணைக்கிறது, எனவே பித்த அமிலங்கள் HMG-CoA ரிடக்டேஸ் மரபணுவின் செயல்பாட்டைத் தடுக்கின்றன. சுமார் 3 இன் தொகுப்பிற்குப் பிறகு HMG-CoA ரிடக்டேஸ் இருப்பதால், இந்த கொழுப்பு நொதியின் தொகுப்பைத் தடுப்பது ஒரு பயனுள்ள ஒழுங்குமுறை ஆகும். |